作者:新纪元 阅读:0
更新时间:2024-04-17 15:52:14发布时间:24小时内
结直肠癌分子检测性能验证
实验室应对待开展的肿瘤基因检测项目需要进行实验室内部验证,如果是使用已经批准的高通量测序试剂,需要进行性能验证,性能验证包括但不限于精密度、准确性、分析敏感性、分析特异性和可报告范围(线性范围)等。
性能验证的时机
1、 检验程序常规应用前
2、 任何严重影响检测系统分析性能的情况发生后,应在检测系统重新启用前对受影响的性能进行部分性能验证。影响检测系统分析性能的情况可包括但不限于仪器主要部件故障,仪器搬迁,设施、环境的严重失控等。
3、 常规使用期间,实验室可基于分析系统的稳定性,利用日常工作产生的检验和质控数据,定期对检验程序的分析性能进行评审,应能满足检验结果预期用途的要求。新检测系统也包含现用检测系统的任一要素(仪器、试剂、校准品等)变更,如试剂升级、仪器更新、校准品溯源性改变等应按照新系统来进行验证。
性能验证的判断标准
实验室应根据临床需求选择经确认的符合预期用途的检验程序。实验室性能验证结果的判断标准是厂商或研发者在试剂盒或检测系统说明书中声明的性能指标。
性能验证的参数
精密度
精密度是指同一样本在多次检测中结果的一致程度,包括重复性和再现性两个方面。
重复性指在同一条件下(相同环境、相同操作人员、相同检测流程、相同仪器)多次测量同一序列,测定结果的一致程度。
再现性指由不同操作人员、不同仪器(相同型号)和不同批试剂进行同一序列测量结果的一致性程度。
准确性
准确性指测定检出的序列与参考序列的一致性程度,对准确性的评价可通过两部分进行。
一是通过检测已知序列的人基因组DNA(如标准细胞株)来评价测序本身的准确性。如果为测序的准确性可通过碱基的正确率来表示;
二是通过检测临床样本进行验证,包括含有疾病相关突变的样本和含有与待检突变相同突变类型的样本,评价范围应包括具有明确临床意义的位点,较难测序或比对的区域、不同GC含量的区域等。

可将NGS与另一已经过确认的方法同时检测临床样本来评价,比较NGS 与另一方法之间结果的差异,不一致的结果再用第三种方法进一步确认,通过阳性符合率(PPA) 和阴性符合率(NPA) 来评价定性测定的准确度。
检测点突变、短片段缺失和短片段插入的比较方法可以采用Sanger 测序、等位基因特异性PCR 等;
检测拷贝数变异的比较方法可以采用实时荧光定量PCR、荧光原位杂交(FISH) 等;
基因融合可采用FISH、实时荧光定量PCR 等,
方法作为NGS 检测的比较方法。
敏感性
敏感性,这里指LoD,通常使用LoD 95%表示,
即有95%的可能性能够正确检出突变位点的最低等位基因百分比。
通常采用已知突变等位基因百分比的样本,用另一基因组DNA ( 或游离DNA) 混合稀释来进行评价。实验室需建立不同突变类型和不同样本类型的LoD 95%。
CNAS-GL039指南中提到,NGS中不同的基因变异类型均应分别进行检测限的验证。且应将待检测变异类型的样本稀释为厂家声明的检测限浓度,以及高于和低于该浓度一个梯度浓度,按照厂家声明的测序深度进行测定,如果≥95%检出限浓度以上的样本检测到可靠变异,则检出限验证通过。
特异性
分析特异性是评价样本中的同源序列或其他交叉反应的序列和内源及外源干扰物质对检测结果的影响。
实验室可根据临床要求、厂家声明和样本特点(实际可能存在的干扰物质及达到的浓度)选择需要验证的干扰物质及浓度。

史上最全癌症靶向及免疫治疗药物清单(含医保覆盖及价格)!
(12)人阅读2023-07-01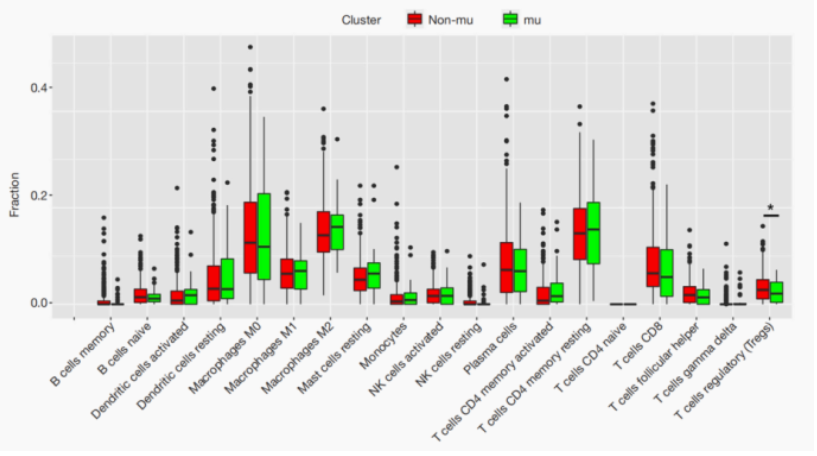
无靶向药可用又遇到PD-L1表达阴性且伴脑转移,却奇迹般的无进展生存近2年!
(1)人阅读2023-07-01
HPV疫苗:确可有效降低宫颈癌患病风险
(0)人阅读2023-07-01
如何避免感染HPV?除了疫苗,还要小心这些.....
(1)人阅读2023-07-01
免疫疗法不起效 原来肿瘤细胞打开“隐身”基因
(0)人阅读2023-07-01
肺癌基因检测?不清楚戳进来
(1)人阅读2023-06-30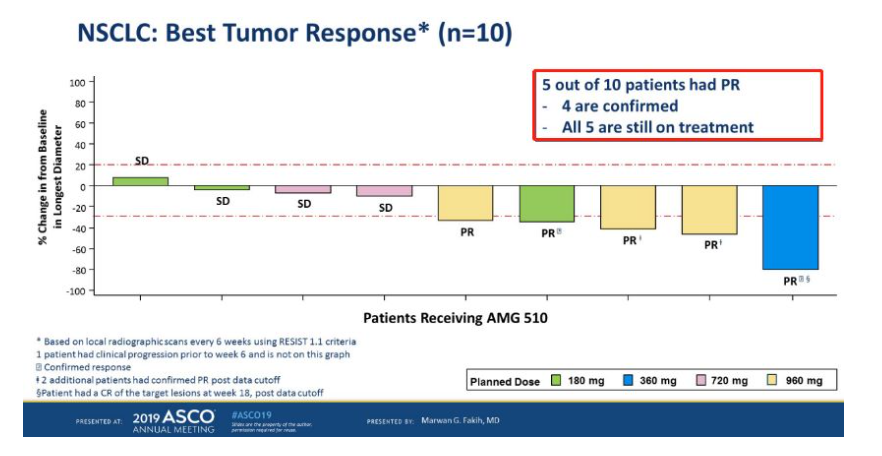
肺癌不只八大基因,六大新基因突变用药来袭,造福更多肺癌患者!
(46)人阅读2023-06-30
HER2检测中IHC与FISH结果不一致是什么原因?
(1)人阅读2023-06-30
为什么查出肺癌做基因检测如此重要?
(0)人阅读2023-06-30
肺癌基因检测攻略(值得收藏!)
(2)人阅读2023-06-30
卵巢癌与基因检测的规范化
(7)人阅读2023-06-28
卵巢癌基因检测怎么选择,不清楚点进来
(2)人阅读2023-06-28